Medivir et Black Earth Farming
Comment expliquez-vous la subite baisse de l’action Medivir ? Constitue-t-elle une opportunité d’achat ?
Dans le dernier article (voir n°39-B) que nous avons consacré à Medivir (83 SEK; ticker MVIRB sur la Bourse de Stockholm; code ISIN : SE0000273294), nous indiquions que le 24 octobre était le jour J pour l’entreprise suédoise. C’est en effet ce jour-là que Medivir devait défendre, en compagnie de Johnson&Johnson – qui détient les droits de vente pour le monde hors Scandinavie -, le dossier d’approbation du simeprevir (TMC435) comme traitement contre le virus de l’hépatite C (VHC) devant la Food&Drug Administration (FDA) américaine. Avec un score parfait de 19 voix contre 0, le panel a recommandé à l’unanimité l’approbation du simeprevir. Mais alors que la FDA accordera normalement cette approbation le 27 novembre, l’action n’a pas été à la fête en Bourse. Une première raison à cela, bien qu’elle ne soit pas neuve, tient au fait que le panel de la FDA recommande que les patients soient d’abord testés sur la présence d’une mutation génétique (polymorphisme Q80K). Les tests cliniques ont en effet révélé que la présence d’une mutation Q80K annihilait l’action du simeprevir. Et la mutation Q80K s’avère être présente chez 48% des membres du principal sous-groupe cible aux Etats-Unis, à savoir les patients présentant le génotype VHC 1a. La deuxième raison, et la principale, est que dès le lendemain, le panel de la FDA a également rendu un avis positif concernant le sofosbuvir du concurrent Gilead Sciences. Le sofosbuvir, qui réduit de moitié la durée de la thérapie par rapport au simeprevir – le traitement passant de 24 à 12 semaines – est également efficace chez les patients présentant la mutation Q80K, mais surtout : le panel a laissé la possibilité d’administrer également du sofosbuvir à des patients déjà traités à l’aide d’autres médicaments. Jusqu’il y a peu, on estimait que ces patients recevraient du simeprevir. En d’autres termes, des doutes sont apparus concernant le potentiel commercial du simeprevir. Le marché des médicaments contre le VHC enregistrera cependant une énorme croissance au cours de la décennie à venir. Selon certaines estimations, il pourrait même atteindre 100 milliards USD ! Le simeprevir avait déjà été approuvé au Japon fin septembre. La demande de commercialisation en Europe est toujours en cours. En outre, plusieurs études sont en cours concernant l’utilisation du simeprevir dans le traitement d’autres types de VHC.
L’action Medivir a été très performante durant les semaines qui ont précédé les décisions des organes de régulation, ce qui nous avait incités à revoir notre avis à la baisse fin septembre. Il est de plus en plus clair que le sofosbuvir présente un meilleur potentiel commercial, avec des ventes attendues de 1,9 milliard USD dès 2014. Mais le simeprevir aura droit à sa part de ce grand gâteau et Medivir en profitera par le biais des royalties sur les ventes. Jusqu’à ce que nous disposions de perspectives plus claires concernant le potentiel commercial du simeprevir et malgré la réaction sans doute excessive du marché, nous maintenons l’avis ” à conserver/attendre ” (3C).
J’enregistre une forte perte virtuelle sur mon investissement dans Black Earth Farming. Vaut-il la peine de faire preuve de patience ou préconisez-vous d’acter mes pertes ?
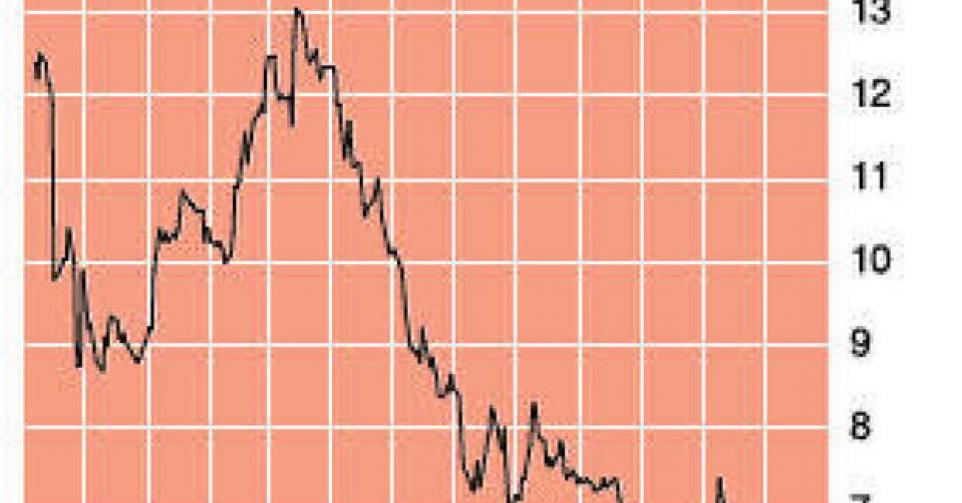
Black Earth Farming (6 couronnes suédoises (SEK); ticker BEF sur le Bourse de Stockholm; code ISIN : SE0001882291) est un propriétaire et exploitant de terres agricoles actif dans la région des Terres noires, dans le sud-ouest de la Russie. Il s’agit de terres agricoles bon marché, mais de bonne qualité, qui sont appropriées à toutes sortes de cultures et présentent encore un fort potentiel de gains de productivité. Les promesses très engageantes exprimées lors de l’introduction en Bourse fin 2007 – prix de souscription : 50 SEK – n’ont jamais été tenues et l’entreprise n’a enregistré un premier bénéfice modeste de 7 millions USD que l’an dernier. Ces dernières années, les Suédois ont beaucoup investi dans une capacité de stockage de 500.000 tonnes afin de pouvoir répondre aux fortes fluctuations des cours des céréales. Par ailleurs, ils ont beaucoup misé sur l’amélioration du traitement et de l’amendement de ces terres agricoles sous-développées. Cet élément avait été sous-estimé, mais la société y travaille et le rendement des cultures devrait s’améliorer au cours des années à venir. Une forte augmentation de capital (65% d’actions nouvelles) a été réalisée fin 2012 avec l’émission de 83,1 millions d’actions à 6,38 SEK par action. L’argent récolté sera affecté à de nouveaux investissements – dans la culture des pommes de terre et des betteraves sucrières – consentis dans le cadre d’un contrat de trois ans conclu par Black Earth avec PepsiCo en octobre 2012. Ce contrat réduira l’exposition à des marchés spots intérieurs particulièrement volatils et pourra prendre à son compte jusqu’à 30% du chiffre d’affaires (CA) d’ici 2015. Au 1er semestre de 2013, Black Earth a limité la perte à 0,5 million USD, contre 11,3 millions USD l’an dernier. L’entreprise réalise normalement la majeure partie de son CA au 2e semestre, mais la nette baisse (20 à 25%) des cours des céréales depuis fin juin est un nouveau contrecoup.
Après un beau début d’année 2013, l’action Black Earth Farming a perdu la moitié de sa valeur depuis mars pour atteindre un plancher historique. A 0,7 fois une valeur comptable conservatrice – les terres agricoles sont actées à une valeur de rachat réduite de 250 USD par action -, les mauvaises nouvelles sont largement intégrées dans le cours. Le contrat avec PepsiCo est un élément positif, mais la pression qui s’exerce sur les cours des céréales nous empêche (provisoirement) de relever notre avis. Nous ne vendrions cependant pas des actions déjà en portefeuille (3C).
Question des lecteurs
Vous avez repéré une erreur ou disposez de plus d’infos? Signalez-le ici




