Galapagos et Vertex Pharmaceuticals
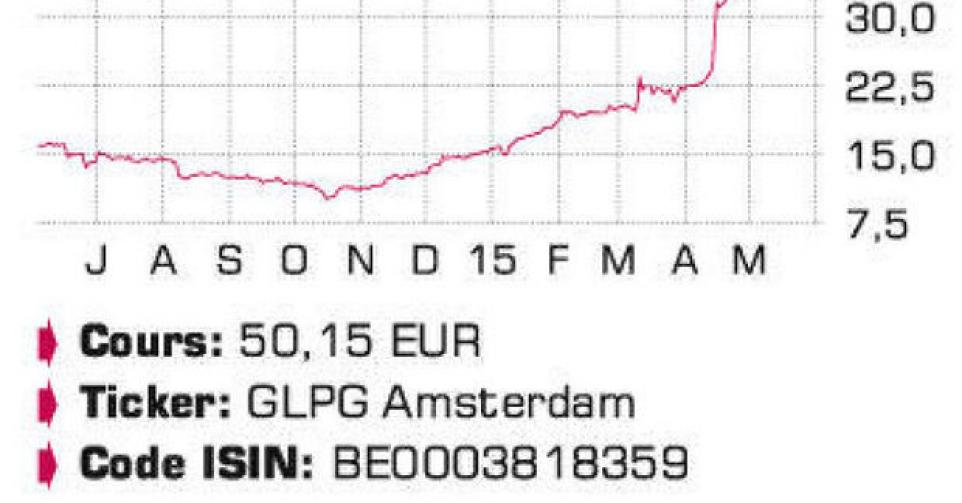
Le cours de l’action Galapagos ne cesse de monter. Suis-je le seul à être pris de vertige ? Ne serait-il pas préférable de vendre ?
L’ascension de l’action de l’entreprise biotechnologique Galapagos (GLPG) est tout bonnement phénoménale. Son cours a en effet quintuplé depuis le plancher d’octobre 2014. La conséquence, bien entendu, des excellents résultats de l’étude de phase IIb sur le filgotinib, l’ancien GLPG0634. Il s’agit d’un inhibiteur de JAK-1 (une protéine active dans les maladies infectieuses) pour lequel GLPG a conclu un deal lucratif avec AbbVie en 2012. Après les excellents résultats intermédiaires (après 12 semaines de traitement) de l’étude DARWIN 1 sur le rhumatisme (594 patients, filgotinib associé à de la méthotrexate), GLPG a pu annoncer des résultats d’efficacité et de sécurité comparables pour DARWIN 2 (283 patients, monothérapie). Les résultats définitifs après 24 semaines de traitement seront publiés en juillet (DARWIN 1) et en août (DARWIN 2). AbbVie décidera ensuite d’une prise en licence du filgotinib (paiement d’étape possible de 200 millions USD), notamment sur la base des résultats, attendus cet été, d’une étude de phase II sur l’ABT-494, son propre inhibiteur de JAK-1. Les résultats d’une étude de phase II sur le filgotinib pour la maladie de Crohn seront également publiés au cours des mois à venir, après quoi AbbVie décidera d’une prise en licence (paiement d’étape de 50 millions USD). La hausse du cours s’est accélérée après l’introduction réussie sur le Nasdaq. GLPG a finalement récolté 279 millions EUR – plus du double de l’objectif initial – via l’émission de 7,5 millions d’actions à 37 EUR et 42,05 USD par action (dilution de 24,4%). AbbVie et Johnson & Johnson y ont notamment souscrit. Un relèvement de l’objectif de cours par UBS (50 EUR) et l’annonce, la semaine dernière, de plusieurs prises de participation dans GLPG après l’IPO ont propulsé l’action à un nouveau record de 55,4 EUR. Avec une capitalisation boursière de 2 milliards EUR, nous estimons la valorisation excessive. GLPG a certes un blockbuster potentiel entre les mains – pic de ventes estimé entre 3 et 5 milliards USD, avec entre 10 et 13% et 20 à 23% de royalties -, mais il faudra encore attendre au moins début 2019 avant de voir le produit sur le marché. GLPG profite très habilement de cette euphorie pour gonfler sa trésorerie et ainsi poursuivre le développement de son pipeline propre. Celui-ci contient notamment une thérapie combinée potentiateur-correcteur comparable (respectivement en phase I et préclinique) à celui de Vertex (voir infra) pour le traitement de la mucoviscidose. L’entreprise étudie également de possibles acquisitions. Après la hausse phénoménale, nous abaissons le conseil à vendre (3C).
Etes-vous comme moi déçu de l’évolution du cours de l’action de Vertex Pharmaceuticals après l’approbation de l’Orkambi par le panel consultatif de la FDA ?
Nous avons en tout cas délibérément repris Vertex Pharmaceuticals dans le portefeuille modèle avant le 12 mai, jour où l’entreprise devait défendre sa thérapie combinée Orkambi devant le panel consultatif. Comme toujours, c’était un jour de grande tension qui s’accompagne de questions relativement critiques concernant l’efficacité (relativement limitée) du produit. Après une réaction initiale positive, l’action est rapidement retombée à son niveau d’avant le 12 mai. L’élément crucial est bien entendu l’avis positif – douze voix pour et une voix contre – concernant l’approbation de l’Orkambi. Après le Kalydeco, le premier produit mis sur le marché par Vertex en 2012, c’est le deuxième produit Vertex pour le traitement de la mucoviscidose. Il s’agit d’une thérapie combinée d’un potentiateur (Kalydeco) et d’un correcteur (Lumacaftor; VX809) pour le traitement d’une forme homozygote de la mutation F508del, la mutation la plus fréquente qui représente 50% de la population ou 20.500 patients de plus de 12 ans aux Etats-Unis et en Europe. Le Kalydeco générera un chiffre d’affaires (CA) compris entre 560 et 580 millions USD (sur la base de maximum 3900 patients) cette année, mais l’Orkambi devrait permettre la grande percée et faire exploser le CA de Vertex à plus de 5 milliards USD d’ici à 2018. La FDA décidera de l’approbation de l’Orkambi le 5 juillet au plus tard. En Europe, la décision tombera au 4e trimestre. A terme, le leader absolu sur le marché du traitement de la mucoviscidose entend traiter des patients de plus en plus jeunes, en raison des dommages pulmonaires structurels beaucoup plus limités à un âge précoce. L’objectif ultime est une thérapie triple (Kalydeco, le correcteur VX661 et un correcteur de deuxième génération à sélectionner cette année) pour le groupe de patients le plus difficile à traiter : la mutation hétérozygote F508del (17.000 patients). Celle-ci transformerait la mucoviscidose en une maladie chronique qui exige une médication tout au long de la vie. Vertex est dès lors le candidat idéal à une acquisition vu sa position unique – plusieurs années d’avance sur la concurrence – et son profil de croissance rapide grâce à un excellent produit dans un syndrome difficile à traiter. Outre Gilead Sciences et Johnson & Johnson, Pfizer a été citée récemment comme repreneur potentiel. Vertex reste dès lors dans le portefeuille modèle (1B).
Question des lecteurs
Vous avez repéré une erreur ou disposez de plus d’infos? Signalez-le ici




