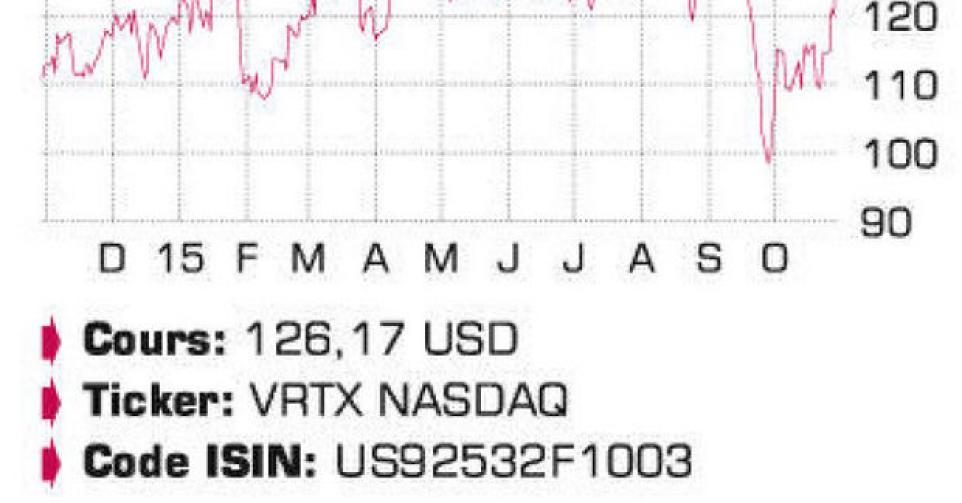
Vertex Pharmaceuticals
Digne d’achat
Nous attendions avec impatience les chiffres relatifs au 3etrimestre de Vertex Pharmaceuticals. C’était en effet le premier trimestre (partiel) de commercialisation d’Orkambi, après l’approbation donnée le 2 juillet par la FDA (l’agence sanitaire américaine). Le groupe espère beaucoup d’Orkambi (ventes maximales attendues de 5 milliards USD), car c’est, après Kalydeco, le deuxième produit qui traite les mutations génétiques responsables de la mucoviscidose. Orkambi est une thérapie de combinaison d’un potentiateur (Kalydeco) et d’un correcteur (Lumacaftor; VX809) destinée au traitement de la forme homozygote de la mutation F508del, une mutation présente chez 8.500 patients de plus de 12 ans aux Etats-Unis et 12.500 patients en Europe. Avec un chiffre d’affaires (CA) de 130,8 millions USD, Orkambi s’est nettement mieux porté que prévu (le consensus se situait entre 75 et 85 millions USD). Fin septembre, plus de 3000 patients étaient déjà en traitement, et la société table déjà sur des ventes maximales au second semestre 2016. Après une recommandation positive, l’approbation d’Orkambi en Europe devrait intervenir au cours de ce trimestre. Le CA de Kalydeco (groupe cible de 3900 patients) a continué de progresser à 165,9 millions USD, soit +31% par rapport au 3etrimestre en 2014 et +8% par rapport au trimestre précédent. Le CA annuel attendu de Kalydeco a progressé à nouveau, de 575 à 590 millions USD à 605 à 620 millions USD. Au 3etrimestre, on note déjà un allègement important de la perte nette, de 170,1 millions USD l’an dernier à 95,1 millions USD, et à partir du 4etrimestre, Vertex sera rentable. Début octobre, la société a présenté une actualisation étendue sur les évolutions du pipeline. La première ambition demeure, à terme, d’atteindre, pour la mucoviscidose, au moins 90% du groupe cible total – 75.000 patients en Amérique du Nord, Europe et Australie. Pour y parvenir, le groupe espère une percée dans le traitement des patients présentant la mutation hétérozygote F508del (17.000 patients), qu’il est le plus difficile de soigner. La société a sélectionné deux nouveaux correcteurs (VX-152 et VX-440), qui seront testés sur les patients à partir de 2016 dans plusieurs thérapies de combinaison triples, avec le potentiateur Kalydeco et le correcteur VX661. L’entreprise a en la matière une avance d’au moins une année sur Galapagos, qui planche, en collaboration avec AbbVie, sur un médicament comparable. Vertex entend du reste améliorer encore son efficacité et organise dans ce cadre quatre études de phase III (une combinaison de Kalydeco et VX661) pour le traitement de différentes mutations. En outre, il développe les épargneurs de potassium (ENaC – P-1037 et P-1055) de Parion Sciences, pour le traitement de la mucoviscidose mais aussi d’autres maladies pulmonaires. Vertex a récemment conclu un accord avec CRISPR Therapeutics pour une étude sur le traitement de maladies génétiques par des modifications génétiques, mais aussi de la grippe (via son partenaire Janssen Pharmaceutica).
Conclusion
Nous sommes très satisfaits des premiers chiffres de vente d’Orkambi. Ce faisant, Vertex confirme le potentiel de croissance énorme de ce marché difficilement pénétrable. La société franchit également des étapes importantes en matière de recherche, mais demeure selon nous un candidat idéal à la reprise.
Conseil: digne d’achat
Risque: élevé
Rating: 1C
Actions américaines
Vous avez repéré une erreur ou disposez de plus d’infos? Signalez-le ici