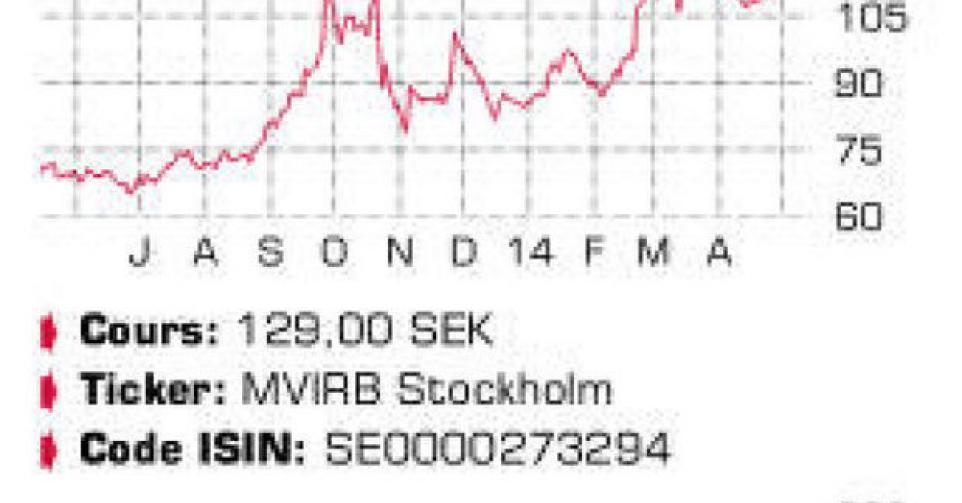
Medivir
Pour l’investisseur conscient des risques
L’entreprise pharmaceutique suédoise a publié d’excellents résultats au terme du 1er trimestre la semaine dernière. C’était le premier trimestre complet depuis la mise sur le marché – par Johnson & Johnson (JNJ; possède les droits de commercialisations mondiaux en dehors de la Scandinavie) – du Simeprevir au Japon, aux Etats-Unis et au Canada à l’automne 2013. Le Simeprevir a atteint au 1er trimestre un chiffre d’affaires (CA) de 354 millions USD, dont 291 millions USD aux Etats-Unis. Des résultats nettement supérieurs aux attentes, puisque les prévisions faisaient état d’un CA de 200 à 800 millions USD pour 2014. Medivir a ainsi empoché 161,7 millions SEK sous forme de royalties, 7,4% du CA. Au 4e trimestre 2013, Medivir avait perçu 10,5 millions SEK. En raison de la douceur de l’hiver passé, les ventes de la division Pharma ont baissé de 9,6% à 46,4 millions SEK. Le CA de 208,2 millions SEK a permis de dégager un bénéfice opérationnel (EBIT) de 88,6 millions SEK. Grâce à un produit fiscal unique de 196,8 millions SEK, le bénéfice net s’est établi à 283,8 millions SEK (9,01 SEK par action). Le bénéfice net récurrent se monte à 87 millions SEK ou 2,78 SEK par action. Simeprevir est un médicament contre l’hépatite C, une maladie du foie causée par le virus de l’hépatite C (VHC) dont souffrent, selon les estimations, 3% de la population mondiale. Le marché des médicaments contre le VHC est appelé à connaître une énorme croissance au cours de la décennie à venir, pour atteindre, selon les estimations, 100 milliards USD. Aujourd’hui, la maladie est combattue à l’aide d’interféron (injection) et de ribavirine. Les médicaments les plus récents sont des inhibiteurs de protéases (comme le Simeprevir; les protéases sont des enzymes qui brisent les protéines et d’autres chaînes d’acides aminés) ou des inhibiteurs de polymérase (comme le Sofosbuvir de Gilead Sciences; les polymérases sont des complexes d’enzymes impliquées dans la propagation du VHC), qui conjuguent une efficacité accrue et une durée de traitement plus brève. JNJ a récemment introduit une demande complémentaire auprès de l’agence américaine de contrôle des médicaments (FDA) pour l’administration conjointe de Simeprevir et de Sofosbuvir sous la forme d’une thérapie orale à prendre une fois par jour pendant huit ou douze semaines. Plusieurs autres études sur des combinaisons de médicaments sont en cours, et des concurrents comme AbbVie et Merck lorgnent également sur le marché. La part de marché du Simeprevir se monte à 20% aux Etats-Unis (Sofosbuvir y est leader absolu) et même à 50% au Japon. Les données de prescriptions hebdomadaires confirment la tendance à la hausse, même s’il est risqué d’extrapoler aveuglément les chiffres de vente. Le Simeprevir a été approuvé en Russie (troisième population de patients souffrant du HCV) en mars et l’approbation définitive en Europe, après une recommandation positive du comité consultatif (CHMP), devrait normalement intervenir en mai. Medivir est prête à commercialiser le Simeprevir en Scandinavie à partir de juin. Une équipe commerciale étendue soutient le lancement de deux nouveaux produits (Adasuve et Suscard) issus de la division Pharma propre depuis avril.
Conclusion
Il faudra certes attendre l’évolution des chiffres de vente du Simeprevir dans un marché des médicaments contre le VHC en évolution rapide, mais nous estimons que même revues à la hausse, les prévisions des analystes pour 2014 – CA de 957 millions SEK et bénéfice par action de 10 SEK – demeurent trop prudentes. Nous reprenons l’action en Sélection. Réservé aux investisseurs conscients des risques !
Conseil: digne d’achat
Risque: élevé
Rating: 1C
Actions européennes
Vous avez repéré une erreur ou disposez de plus d’infos? Signalez-le ici