De nombreux mois cruciaux pour Sequana Medical
Refinancée, l’entreprise peut poursuivre ses études et le développement de sa solution DSR durant de nombreux mois. Elle devrait pouvoir convaincre de nouveaux investisseurs, et voir son action se réapprécier.
La spécialiste gantoise du traitement des ascites a levé le 7 mars 28,4 millions d’euros, par l’émission de 5,17 millions de nouvelles actions à 5,5 euros l’unité, soit sans décote par rapport au dernier cours avant la suspension – mais l’action avait perdu 15-20% de sa valeur au cours des semaines précédentes, dans un contexte boursier peu avenant. Le nombre d’actions en circulation a augmenté de 27,8%. Grâce à ce nouveau financement, Sequana Medical peut poursuivre ses activités sereinement jusqu’au 2e trimestre de 2023. Cette période sera marquée par un flux abondant de nouvelles importantes.
Au 4e trimestre de 2022 seront publiés les résultats des principaux critères d’évaluation de l’étude POSEIDON, menée en Amérique du Nord, qui teste l’alfapump, la pompe qu’a développée l’entreprise pour recueillir les ascites, chez des patients recrutés fin 2021 qui présentent une accumulation récurrente de liquide dans l’abdomen en raison d’une maladie du foie. Les résultats intermédiaires, publiés début juillet 2021, lesquels portaient sur une cohorte non randomisée de (26) patients, étaient très encourageants. Si les prochains sont concluants, Sequana soumettra sa demande d’autorisation de mise sur le marché mi-2023. L’entreprise entend se charger de la commercialisation de l’appareil en toute autonomie. Elle cible les quelque 150 centres de transplantation du foie que comptent les Etats-Unis. L’alfapump est également évaluée sur des patients atteints d’insuffisance cardiaque qui souffrent de graves problèmes de rétention de liquide malgré la prise de diurétiques; le recrutement des patients pour l’étude SAHARA DESERT devrait être terminé au 2e trimestre, et les résultats suivront dans la seconde moitié de l’année. Cette étude de sécurité et de faisabilité évalue l’effet de l’alfapump DSR (élimination directe du sodium) sur 20 patients atteints d’insuffisance cardiaque chronique dont l’équilibre sodium-liquide n’est pas sous contrôle (congestion), en dépit de la prise de hautes doses de diurétiques. Les résultats intermédiaires, annoncés en décembre, étaient excellents. Le recours répété à l’alfapump DSR a permis de mettre un terme, de manière sûre, efficace et rapide, à la congestion persistante chez les six premiers patients, sans avoir à leur administrer de diurétiques. Par ailleurs, leurs symptômes d’insuffisance cardiaque ont été réduits de 30% et leur fonction rénale est restée stable, alors que jusqu’ici, avec ce type de traitement, une détérioration de celle-ci était la norme. De surcroît, après la première phase de traitement intensif, les patients ont réagi aux diurétiques presque comme des personnes saines. Les effets secondaires, limités, ont été traités facilement.
Parallèlement à ces études, Sequana développe sa solution DSR brevetée de nouvelle génération (DSR Infusate 2.0). Elle présentera les données précliniques à ce sujet au 2e semestre de 2022, avant, espère-t-elle, de conduire une première étude clinique aux Etats-Unis (MOJAVE), dont les résultats seraient dévoilés mi-2023. Après quoi elle se mettrait en quête d’un partenaire pour une étude sur l’insuffisance cardiaque. Au 2e semestre de 2023 devrait commencer un autre essai clinique aux Etats-Unis, qui évaluera à la fois l’alfapump et la solution DSR.
Sequana s’est vu octroyer une certification majeure (MDR) pour son alfapump en février, après en avoir déjà obtenu une pour son système de gestion de la qualité sur le marché américain, entre autres, en novembre 2021.
Conclusion
L’action, qui avait piqué du nez à l’approche de l’augmentation de capital, s’est légèrement redressée depuis. Le flux de nouvelles attendues dans les 18 prochains mois devrait convaincre un plus grand nombre (d’Américains) d’investir dans Sequana et permettre un partenariat dans le domaine de l’insuffisance cardiaque. Nous y croyons, et tablons sur une revalorisation de l’action, qui reste dans le portefeuille modèle.
Conseil: acheter
Risque: élevé
Rating: 1C
Cours: 6,18 euros
Ticker: SEQUA BB
Code ISIN: BE0974340722
Marché: Euronext Bruxelles
Capit. boursière: 134 millions EUR
C/B 2021: –
C/B attendu 2022: –
Perf. cours sur 12 mois: -26%
Perf. cours depuis le 01/01: -19%
Rendement du dividende: –
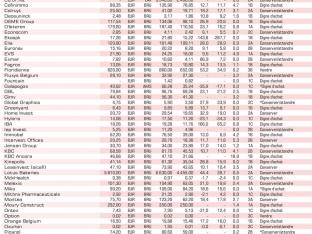
Actions belges
Vous avez repéré une erreur ou disposez de plus d’infos? Signalez-le ici